第七章 沉淀滴定法
考试大纲要求
1.掌握:莫尔法、佛尔哈德法及法扬司法指示终点的基本原理、滴定条件和应用范围;
2.熟悉:沉淀滴定法的基本理论;
3.了解:沉淀滴定法对沉淀的要求;沉淀滴定法在药学领域的应用。
内容提要
1.沉淀滴定法的基本内容;
沉淀滴定法主要讨论银量法:(1)银量法的基本原理;(2)铬酸钾指示剂法、铁铵钒指示剂法和吸附指示剂的基本内容指示终点的原理、滴定条件和应用范围。
【配套练习】
一、名词解释
1.银量法
2.铬酸钾指示剂法
3.铁铵钒指示剂法
4.吸附指示剂法
二、填空题
1.法扬司法中吸附指示剂的Ka愈大,适用的pH愈 ,如曙红(pKa=2.0)适用的pH为 。
2.铬酸钾法测定NH4Cl中Cl-含量时,若pH>7.5会引起 的形成,使测定结果偏 。
3.沉淀滴定法中,铁铵钒指示剂法测定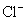 时,为了防止AgCl沉淀的转化需加入 。
时,为了防止AgCl沉淀的转化需加入 。
4.法扬司法测定Cl-时,在荧光黄指示剂溶液中常加入淀粉,其目的是保护 ,减少凝聚,增加 。
5.铁铵钒指示剂法既可直接用于测定 离子,又可间接用于测定各种 离子。
6.铁铵钒指示剂法既可直接用于测定 离子,又可间接用于测定各种 离子。
7.AgCl在0.01 mol/l HCl溶液中的溶解度比在纯水中的溶解度小,这是 效应起主要作用。若Cl-浓度增大到0.5 mol/l,则AgCl的溶解度超过纯水中的溶解度,这是 效应起主要作用。
三、 选择题
1.若A为强酸根,存在可与金属离子形成配合物的试剂L,则难溶化合物MA的溶解度计算式为: ( )
A.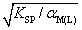 B.
B.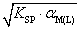
C.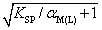 D.
D.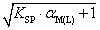
2.在法扬司法测Cl-,常加入糊精,其作用是: ( )
A.掩蔽干扰离子 B. 防止AgCl凝聚
C.防止AgCl沉淀转化 D. 防止AgCl感光
3.铬酸钾指示剂法,如按理论量加入指示剂造成:( )
A. 滴定终点提前 B. 黄色太深,终点推迟
C. 滴定误差最小 D. 无法确定终点
4.下列离子能用铬酸钾指示剂法测定的是:( )
A. Cl- B. Ag+ C. SCN- D.I-
5.Mohr法不能用于碘化物中碘的测定,主要因为: ( )
A. AgI的溶解度太小 B. AgI的吸附能力太强
C. AgI的沉淀速度太慢 D. 没有合适的指示剂
6.用Mohr法测定Cl-,控制pH=4.0,其滴定终点将:( )。
刚好等于化学计量点
7.AgNO3滴定液应贮存于: ( )
A.白色容量瓶 B.棕色试剂瓶
C.白色试剂瓶 D.棕色滴定管
8. 铬酸钾指示剂法测定NaCl含量时,其滴定终点的现象是: ( )
A.黄色沉淀 B.绿色沉淀
C.淡紫色沉淀 D.浅的砖红色沉淀
9.AgCl比Ag2CrO4先沉淀的原因是: ( )
A. AgCl颗粒比Ag2CrO4小 B. AgCl溶度积比Ag2CrO4小
C. AgCl溶解度比Ag2CrO4小 D. AgCl溶解度比Ag2CrO4大
10.吸附指示剂法使用的滴定液为:( )
A. NH4SCN B. KSCN C. K2CrO4 D.AgNO3
11.铁铵矾指示剂法测定下列哪一种离子时,应防止沉淀转化:( )
A. Ag+ B. Cl- C.I- D.Br-
12银量法分类的依据是( )不同。
A. 滴定液 B. 生成的沉淀 C.指示剂 D.分析对象
四、计算题
1.称取NaCl基准试剂0.1773 g,溶解后加入30.00 mLAgNO3标准溶液,过量的 Ag+ 需要3.20 mLNH4SCN标准溶液滴定至终点。已知20.00 mL AgNO3标准溶液与21.00 mL NH4SCN标准溶液能完全作用,计算AgNO3和NH4SCN溶液的浓度各为多少? (已知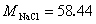 )
)
2.用铁铵矾指示剂法测定0.1 mol/L的Cl-,在AgCl沉淀存在下,用0.1 mol/L KSCN标准溶液回滴过量的0.1 mol/LAgNO3溶液,滴定的最终体积为70mL,[Fe3+]=0.015 mol/L。当观察到明显的终点时,([FeSCN2+]=6.0×10-6 mol/L),由于沉淀转化而多消耗KSCN标准溶液的体积是多少?(已知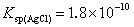 ,
,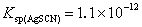 ,KFeSCN = 200)
,KFeSCN = 200)
参考答案
一、名词解释
1.银量法:利用生成难溶性银盐反应的沉淀滴定法成为银量法。
2.铬酸钾指示剂法:以铬酸钾(K2CrO4)为指示剂的银量法。
3.铁铵钒指示剂法:以铁铵矾(NH4Fe(SO4)2·12H2O)为指示剂的银量法。本法分为直接滴定法和返滴定法。
4.吸附指示剂法:以吸附剂为指示剂的银量法。
二、填空题
1.低,≥2.0
2. Ag(NH3)2+;高
3.硝基苯
5.胶体;吸附
6.Ag+;卤素
7.同离子;配位
三、选择题
1.B;2.B;3.B;4.A;5.B;6.C;7.B;8.D;9.D;10.D;11.B;12.C;
四、计算题
1.解:过量AgNO3的体积 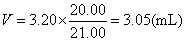
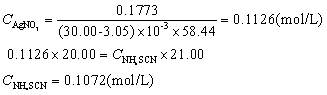
2. 解: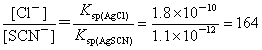
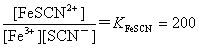
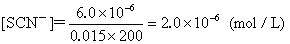
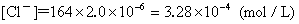
设多消耗KSCN的体积为V mL,则
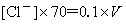
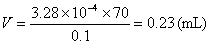
 通知公告
通知公告

 友情链接:
友情链接: