一、名词解释(每小题4分,共20分)
1.系统误差
2.标准溶液
3银量法
4.Lambert-Beer定律
5.电位滴定法
二、填空题(每空1分,共20分)
1. 有机化学分析不仅有元素分析,还有 和 分析。
2. 有效数字的修约采用 规则。
3. 在EDTA七种形式中,只有_______才能与金属离子直接生成稳定的配合物。
4. 法扬司法测定Cl-时,在荧光黄指示剂溶液中常加入淀粉,其目的是保护 ,减少凝聚,增加 。
5.标定硫代硫酸钠一般可选_______ 作基准物,标定高锰酸钾溶液一般选用_____ __作基准物。
6.碘在水中的溶解度小,挥发性强,所以配制碘标准溶液时,将一定量的碘溶于_______溶液。
7.电位固定不变,不受溶液组成变化影响的电极称为参比电极。常用的参比电极为______ ___和______ ___两种。
8.pH玻璃电极在使用前需要在纯水中浸泡__ ____以上,
目的是___ __ ___。
9.可见光的波长范围为 ,近紫外分光的波长范围为 。
10. 在光度分析中,常因波长范围不同而选用不同材料制作的吸收池。可见分光光度法中选用__________吸收池;紫外分光光度法中选用__________吸收池;红外分光光度法中选用__________吸收池。
11. 标定硫代硫酸钠一般可选_______作基准物,标定高锰酸钾溶液一般选用_______作基准物。
三、选择题(每小题2分,共30分)
1. 在非水酸碱滴定中,常使用高氯酸的冰醋酸溶液。为了除去水分,需加入适量的( )
A.醋酐 B.无水CaCl2 C.醋酸汞 D.乙醚
2. 测定0.2mg样品中被测组分的含量,按取样量的范围应为:( )
A.常量分析 B.半微量分析 C.超微量分析 D.微量分析
3. 在不加样品的情况下,用测定样品同样的方法、步骤,对空白样品进行定量分析,称之为( )
A、对照试验 B、平行试验 C、空白试验 D、预试验
4. 朗伯-比耳定律适用于()
A.非单色光 B.介质的不均匀 C. 单色光 D.溶液浓度较高
5. 下列关于副反应系数的定义,正确的是( )。
A. 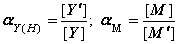 B.
B. 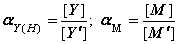
C. 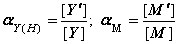 D.
D. 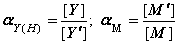
6. 工作要求测定结果的误差应( )。
A、愈小愈好 B、等于零 C、没有要求 D、在允许误差范围内
7. EDTA与金属离子形成配合物时,其配位比为( )。
A、1:1 B、1:2 C、2:1 D、1:6
8.不能用莫尔法测定的离子是( )
A、Cl- B、Br- C、Ag+ D、SCN-和I-
9. 下列各项叙述中不是滴定分析对化学反应要求的是( )。
A. 反应必须有确定的化学计量关系 B. 反应必须完全
C. 反应速度要快 D. 反应物的摩尔质量要大
10. 根据试样用量的多少,试样用量在 0.1g 以上的属于: ( )
A、超微量分析 B、半微量分析 C、微量分析 D、常量分析
11. 在金属离子M和N等浓度的混合液中,以HIn为指示剂,用EDTA标准溶液直接滴定其中的M而N不干扰,要求( )
A、pH=pK’MY B、pK’MY < pK’MIn
C 、lgK’MY –lgK’NY≥5 D、MIn与HIn颜色应有明显的区别
12.在含有AgCl沉淀的溶液中,加入氨水,将使AgCl沉淀的溶解度增大,这种效应属于( )
A、同离子效应 B、盐效应 C、酸效应 D、配位效应
13.KMnO4法应用( )
A、自身指示剂 B、外指示剂 C、金属指示剂 D、吸附指示剂
14. 0.01mol·L-1某一元弱酸能被准确滴定的条件是( )
A、Ka≥10-8 B、Ka≥10-6 C、Kb≥10-6 D、Kb≥10-8
15. 间接碘量法中加入淀粉指示剂的适宜时间是( )
A、滴定开始前 B、滴定开始后
C、滴定至近终点时
D、滴定至红棕色退尽至无色时
四、四、计算题(每小题10分,共30分)
1. Lambert-Beer定律的物理意义是什么?为什么说Beer定律只适用于单色光?浓度C与吸光度A线性关系发生偏离的主要因素有哪些?(10分)
2.用配位滴定法测定氯化锌(ZnCl2)的含量。称取0.2500g试样,溶于水后,稀释至250ml,吸取25.00ml,在pH=5~6时,用二甲酚橙作指示剂,用0.01024 mol·L-1 EDTA标准溶液滴定,用去17.61ml。试计算试样中含ZnCl2的质量分数?(10分)
3.安络血的相对摩尔质量为236,将其配成100 mL含安络血 0.4300 mg的溶液,盛于1 cm吸收池中,在λmax=55 nm处测得A值为0.483,试求安络血的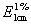 和ε值。(10分)
和ε值。(10分)
参考答案
一、名词解释(每小题4分,共20分)
1.系统误差由某种确定的原因所引起的误差,一般有固定的方向(正负)和大小,重复测定时重复出现
2.标准溶液:已知准确浓度的试剂溶液。
3.银量法:利用生成难溶性银盐反应的沉淀滴定法成为银量法。
4.Lambert-Beer定律:当一速平行单色光通过均匀的非散射溶液时,溶液对光的吸光度与溶液的浓度及厚度的乘积成正比。
5.电位滴定法:应用滴定方法根据滴定过程电极电位的变化确定滴定终点求算被测物的含量的方法。
二、填空题(每空1分,共20分)
1. 官能团、分子。2. 四舍六入五留双
3. [Y4-]。4.胶体,吸附。5. 重铬酸钾;草酸钠。
6. 碘化钾。
7. 饱和甘汞电极;氢电极。8. 24 h, 减少不对称电位。
9. 400nm-760nm; 200nm-400nm。
10. 玻璃;石英;岩盐。 11.重铬酸钾;草酸钠。
三.选择题(每小题2分,共30分)
ADCCC DADDD CDABC
四、简答、计算题(每小题10分,共30分)
1. (10分)答:朗伯-比耳定律的物理意义:当一束平行单色光垂直通过某溶液时,溶液的吸光度A与吸光物质的浓度c及液层厚度l成正比。
Beer定律的一个重要前提是单色光。也就是说物质对单色光吸收强弱与吸收光物质的浓度和厚度有一定的关系。非单色光其吸收强弱与物质的浓度关系不确定,不能提供准确的定性定量信息。浓度C与吸光度A线性关系发生偏离的主要因素
(1)定律本身的局限性:定律适用于浓度小于0.01 mol/L的稀溶液,减免:将测定液稀释至小于0.01 mol/L测定
(2)化学因素:溶液中发生电离、酸碱反应、配位及缔合反应而改变吸光物质的浓度等导致偏离Beer定律。减免:选择合适的测定条件和测定波长
(3)光学因素:非单色光的影响:减免:选用较纯的单色光;选lmax的光作为入射光
杂散光的影响:减免:选择远离末端吸收的波长测定
散射光和反射光:减免:空白溶液对比校正。
非平行光的影响:减免:双波长法
2.(10分)解:
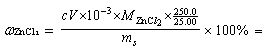
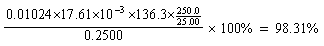
3. (10分) 解:由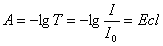
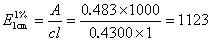 (mL/g×cm)
(mL/g×cm)
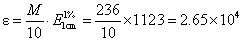 (L/mol×cm)
(L/mol×cm)
 通知公告
通知公告

 友情链接:
友情链接: